|
甄长红 版权所有
|
|
copyright 1991-2019 青果园电厂化学资料网 ( www.qgyhx.cn ) All rights reserved 陇ICP备09001450号 |

随着燃料电池在电动车、可移动电源等方面的应用,需要制氢设备能够方便灵活地在线供氢。由此产生了一种由甲醇部分氧化和蒸汽重整结合在一起的重整方式,即采用甲醇在线制氢时,可首先进行(2) 式所示的氧化重整反应。由于反应本身放热,可以实现氢气生产的冷启动,迅速释放氢气,实现即时供给[9 ] 。当系统温度升高以后,采用(3) 式所示的蒸汽重整方式,可使氢气产率迅速提高。由于(2) 、(3)分别为放热和吸热反应,因此可以互补,从而使体系的热量得到充分利用,达到热平衡。在这一过程中,75 %的氢气被收集,剩下25 %的氢气则返回重整器,用作燃料来提供热量[8 , 26 ] 。而当这一重整方式与PEMFC 联用时,PEMFC 的尾排氢气也可以返回重整器进行再利用,通过燃烧的方式来提供蒸汽重整所需的一部分热量,从而使总的氢气利用率得到大
幅度提高。
三、生物质制氢
生物质制氢可以将低能量密度的生物质能转化为储运方便的高品质氢能。这种方法虽然采用生物质作为制氢原料,但与生物制氢不同的是,所用的制氢方法是化学方法。这种方法利用亚临界或超临界水强大的溶解力,将生物质中的各种有机物溶解,生成高密度、低粘度的液体,再经高温高压处理,可使生物质气化率接近100 %。
虽然高浓度的生物质在生产中更具有经济性和吸引力,但在气化过程中容易发生分解产物的聚合,因此低浓度的生物质比前者更容易气化。为了解决高浓度生物质的气化问题,采用活性炭[13 ] 或Ni 催化剂[14 ] 都可以提高生物质的气化率,但气化后甲烷的产率得到提高,而氢气的产生却受到抑制。进一步的研究发现[15 ] ,由于碱的存在可促进气体的转化反应(4) ,因而在有少量碱存在的情况下,氢气的产率可比没有碱时提高3 倍。
CO + H2O ZCO2 + H2 (4)
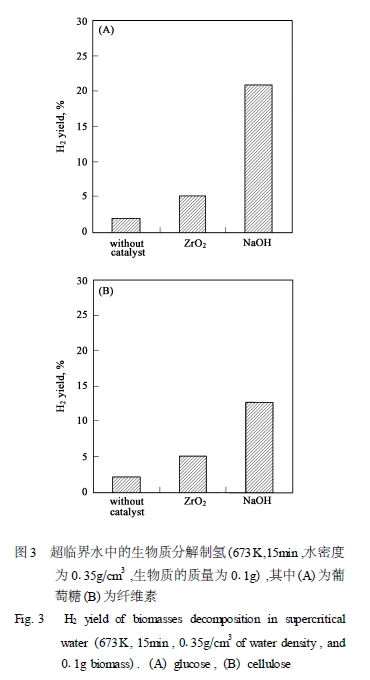
但是,当采用强碱作为催化剂时,其回收再利用存在着很大的不便,增加了反应的成本。而采用固体催化剂则可以方便地实现回收。Watanabe 等[16 ]发现ZrO2 等氧化物可以于超临界水中稳定地存在,并且具有良好的催化性能,生物质的气化效率为不使用催化剂时的两倍。
不过,如图3 所示,生物质制氢的氢气产率还比较低,而且由于超临界水具有极强的腐蚀性,对生物质制氢设备的材质提出了很高的要求;要使超临界水进行气化又必须高温高压的反应条件。这些都对生物质制氢的规模应用提出了挑战。
四、金属置换制氢
当金属与水或酸反应时,就可以置换出氢气。
新鲜切割的金属表面具有很高的反应活性,可以与水反应产生气泡。Uehara 等人[27 ] 的研究表明,当铝
或铝合金在水中被切割或碾碎的时候,可以持续地释放出氢气。反应主要按照(5) 、(6) 所示的两种方式进行。由反应的吉布斯自由能可以看出, (5) 、(6)均为自发反应。当机械切割行为停止时,放氢反应也会立刻终止,从而实现氢气的即时供应。为了使金属能够完全参与反应,需要在水中用高速旋转的飞轮将金属块磨得很细。
2Al + 3H2O Al2O3 + 3H2
ΔG = - 43512 kJPmol (5)
2Al + 6H2O 2Al (OH) 3 + 3H2
ΔG = - 44411 kJPmol (6)
当以燃料电池发动机来驱动轿车的时候,行使250km需要消耗2kg 的氢,所需要的制氢原料消耗量分别为:汽油20L ,或甲醇13kg ,或铝18kg。因此,从成本上看,采用金属铝给燃料电池车供氢并不占优势。但这种制氢方法具有安全、可控、反应器成本低、无污染、可回收等特点,使其得到一定的关注。
如果要将金属置换制氢成功地应用到燃料电池车中, 则还需要解决金属还原再利用的问题。
Otsuka 等人[28 ] 利用天然气重整所得到的CO、H2 混合气对金属氧化物进行还原;然后将金属与水进行
反应,释放出氢气,由此达成一个良性循环。他们利用Fe 和Fe3O4 的氧化还原反应来实现这种过程,并希望以此为燃料电池车提供新的储存和供应氢气的办法。不过反应需要在300 ―400 ℃的温度下进行,经过3 次循环后,放氢速度明显减慢。通过在Fe3O4中添加Ga 、V、Cr 、Mo 、Al 、Ti 、Zr 等其他金属的氧化物,可以有效地增大其比表面,使放氢反应保持较高的速度。
五、太阳能制氢
将太阳能转化为氢能可以形成一种良性循环的能源体系。科学家已经描绘出了一种理想的氢能体系:利用太阳能分解水,再通过燃料电池将产生的H2 和O2 进行电化学反应,产生电能;副产物水又可作为太阳能制氢的原料。整个体系实现了完美的循环,而且对环境没有任何污染。
11 光解水制氢
目前,利用太阳能制氢主要有光解水制氢和氧化物还原制氢两种方式。
由于水是一种稳定的化合物,其分解是非自发的,因此利用光能分解水必须要有催化剂的参与。
作为一种很有吸引力的制氢方式,光解水制氢还存在着一些问题:
(1) 可见光的利用。相当多的研究使用以TiO2[17 , 18 ] 、ZrO2[19 , 20 ] 、SrTiO3[21 ] 等为主的氧化物催化剂,但激发光源主要为紫外光,且光解效率不高。为了能够利用可见光进行光解水,一些研究者采用
CdO[22 ] 、CdS[23 ] 等对层状氧化物进行修饰。修饰后的复合催化剂不仅光催化活性得到提高,而且将其
光谱影响扩大到了可见光范围。另外,Cu2O 在可见光范围内分解水的稳定性很好,并且由于压电现象的存在而具有机械助催化的性质。
(2) 催化剂的光腐蚀。CdS 修饰虽然能明显提高催化剂性能,但由于CdS 属于窄禁带半导体材料,具有光腐蚀作用,尤其是对可见光敏感,因此其应用受到了限制。
(3) 能量转化效率不高。采用氧化物催化剂产生光活性电荷的效率往往不高,难以达到足够的电荷浓度来引发水的分解。这是由于半导体材料在光的激发下产生的自由电子和空穴很容易进行再复合,从而使光催化活性下降。一种解决办法是在保证活性的前提下,增大活性点之间的距离。Liu 等人[20 ]采用高比表面的多孔MCM241 分子筛作为载体,担载ZrO2 作为活性物。由于将催化剂高度分散,降低了光激发电子和空穴再复合的几率,其光催化效率比未担载的ZrO2 提高了215 倍。另一种办法是在光解过程中引入电子给体,使之与空穴或者O2 结合,发生不可逆反应,从而保证光活性的电荷不被消耗。Li 等人[18 ] 利用有机废水中的草酸等作
为电子给体进行了实验探索。
(4) 逆反应的存在。为降低制氢过程中的过电势,可将Pt 等金属担载于TiO2 等氧化物半导体上。
但由于产生的H2 和O2 很容易在金属Pt 上化合,而且H2 和O2 生成H2O 的反应在常温常压下就能达到热力学平衡,因此Pt2TiO2 催化剂很难直接将纯水转变为H2 和O2 。Abe 等人[29 ] 发现, IO3- 或I- 离子能够阻碍逆反应的进行,从而保证正反应的顺利进行。Lee 等人[30 ] 将适量KI 加入到KOH 碱性水溶液中,研究了KI 和KOH 浓度对光解过程的影响,并将优化后的铂担量定为0175wt %。
21 氧化物还原制氢
另一种利用太阳能制氢的方法是将金属氧化物还原,再将金属与水反应产生氢气。金属可以通过燃烧产生热量,或通过燃料电池和化学电源产生电能,或通过水分解反应产生氢气,因而是一种很有潜力的储存和运输能量的方式。然而,经历上述途径产生能量后,金属都会变成氧化物的形式,需要被重新还原才能循环使用。传统的还原方式是碳热还原或电化学还原,耗能较高。而利用太阳能还原则既能降低能源消耗,又能减少对环境的污染。
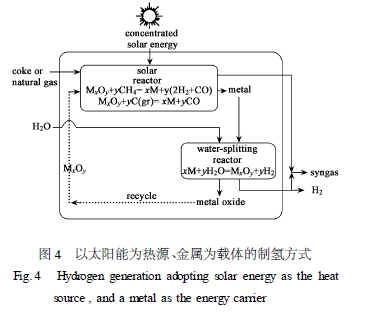
采用两步反应的回路模式[31 ] ,就可以更好地利用太阳能来产生氢能,从而减少化石燃料的消耗和污染物的排放。首先在焦炭和天然气等还原物质的作用下,利用太阳能产生的热量,通过吸热反应,将金属氧化物还原到更低的氧化态或是金属;然后再经历一个放热过程,使低氧化态的金属氧化物或金属与水反应,产生氢气。副产物金属氧化物作为能量载体,经回收后参与下一次的还原反应;所产生的氢气中,大部分被储存起来,一小部分可以用作下一次循环的还原气,如图4 所示。由此,以金属的氧化2还原反应为桥梁,实现了太阳能到氢能的转化。
 最新评论
最新评论|
甄长红 版权所有
|
|
copyright 1991-2019 青果园电厂化学资料网 ( www.qgyhx.cn ) All rights reserved 陇ICP备09001450号 |